Etiketten für die Pharmazeutische Industrie – FMD-konform
DataMatrix-Codes, die am Point of Sale verifiziert werden – nicht nur in der Produktion.
Pharmazeutische Etiketten auf Glas, Kunststoff und Blister stellen Anforderungen, die Standard-Haftsysteme nicht erfüllen. Cryo-Etiketten, Mehrlagen-Etiketten und autoklavierbare Varianten halten Sterilisationszyklen, Tiefkühllogistik und EMVS-Verifikation stand – dokumentiert nach FMD, AMG § 10 und GMP.
Code korrekt gedruckt – Apotheke kann nicht scannen.
Die FMD-Verifikation scheitert nicht im IT-System. Sie scheitert, wenn der DataMatrix-Code auf dem Etikett einen zu geringen Kontrast hat, scharfe Kanten fehlen oder das Folienmaterial unter Transportbedingungen nachgibt. Das Ergebnis: Die Verpackung gilt am Point of Sale als nicht verifizierbar.
Ein nicht lesbarer Code bedeutet kein administratives Problem. Er bedeutet Marktsperrung der betroffenen Charge. Jede Einzelpackung, die das EMVS nicht verifizieren kann, darf nicht abgegeben werden. Der Rückruf folgt nicht irgendwann – er folgt sofort, wenn die erste Apotheke den Scan verweigert.
Das Risiko beginnt nicht beim falschen Dateninhalt. Es beginnt beim Etikett selbst: Haftverlust auf Borosilikatglas nach Kühlkettenpassage, Druckdegradation nach Sterilisationszyklen oder Delaminierung durch Kondensat. Wer diese drei Ebenen nicht gemeinsam adressiert, löst das Problem nicht.

Drei Ebenen gleichzeitig beherrschen – nicht nacheinander
Pharmazeutische Kennzeichnung funktioniert nur, wenn Druck, Material und Systemanbindung von Anfang an zusammen geplant werden. Wer das Etikett erst nach der Anlagenspezifikation auswählt, verliert Spielraum bei Substraten und Prozessparametern. Wir kennen die Abhängigkeiten zwischen Etikettiersystem, Verpackungssubstrat und Serialisierungsschnittstelle – und bringen dieses Wissen in die Auswahl ein, bevor Ihre Linie läuft.
Substrat-Kompatibilität vor Serienstart
DataMatrix-Qualität als Druckprozess
Validierbarkeit als Planungsgröße
Mehrsprachigkeit und Flächeneffizienz planen
Untergrund-Kompatibilität
• Haftet auf Borosilikatglas, PE, PET und Aluminiumfolie – auch ohne Oberflächenvorbehandlung.
• Bleibt stabil auf Blisterkavitäten bis zur letzten Einheit, ohne an den Kavitätenkanten nachzugeben.
• Funktioniert auf Kryoröhrchen aus Polypropylen auch nach mehrfachem Gefrieren und Auftauen.
Chemische Resistenz
• Hält Isopropanol und Ethanol in Konzentrationen bis 70 % stand – bei Desinfektionsroutinen in Produktion und Logistik.
• Zeigt keine Quellung oder Haftverlust bei pH-Werten zwischen 2 und 12, relevant für CIP-Reinigungszyklen.
• Besteht gegenüber organischen Lösungsmitteln wie Aceton und MEK – auch in Laborumgebungen mit direktem Kontakt.
Thermische Belastbarkeit
• Übersteht Dampfsterilisation bei 121 °C und 134 °C ohne Dimensionsveränderung oder Druckdegradation.
• Hält Tiefkühltemperaturen bis in den Flüssigstickstoff-Bereich durch – ohne Delaminierung bei Kondensation.
• Bleibt bei Ethylenoxid-Sterilisation formstabil, Druck und Klebkraft verändert sich dabei nicht.
Mechanische und Witterungs-Exposition
• Übersteht mechanische Belastung im Palettentransport, der DataMatrix-Code bleibt maschinell lesbar.
• Hält Abrieb durch Förderanlagen und Handhabung in der Logistikkette durch – gemäß ISO/IEC 16022 bis 30 % Beschädigung lesbar.
• Zeigt keine Druckablösung bei dauerhafter Feuchtigkeitseinwirkung in der Kühlkette.
Technisches Leistungsprofil pharmazeutischer Etiketten
Pharmazeutische Etiketten durchlaufen mehr als die Verpackungslinie. Sie überstehen Sterilisationszyklen, Tiefkühllogistik, Desinfektionsroutinen und mechanische Belastung im Transport – auf Substraten, die für Standard-Haftsysteme problematisch sind. Das Folienmaterial, der Klebstoff und die Druckschicht bilden dabei ein System. Jede Komponente ist auf die Belastungen abgestimmt, die in der pharmazeutischen Produktion und Lieferkette real auftreten: von der Abfülllinie bis zur Apothekenausgabe. Die folgenden Parameter beschreiben, was dieses System in der Praxis leistet.
Fünf Etikettentypen für pharmazeutische Anforderungen
Nicht jede Anwendung in der Pharmaproduktion stellt dieselben Anforderungen. Die folgenden fünf Etikettentypen decken die kritischsten Einsatzbereiche ab – von der Tiefkühllogistik bis zum integrierten Beipackzettel auf der Primärverpackung.
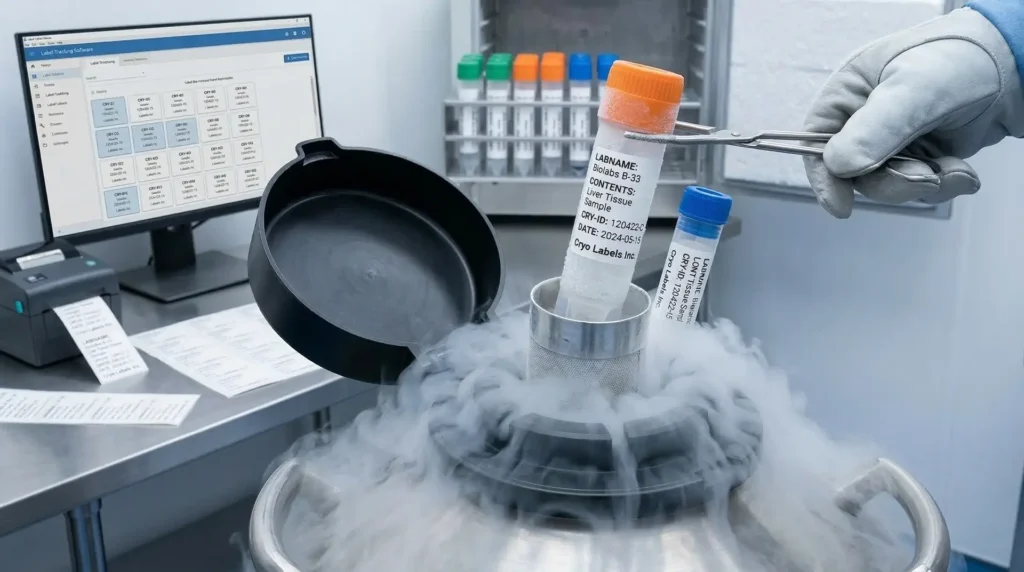
Cryo-Etiketten
Biologika, Impfstoffe und klinische Studienmaterialien lagern bei Temperaturen, bei denen normaler Klebstoff innerhalb von Stunden abfällt. Cryo-Etiketten haften auf Kryoröhrchen und Glas-Vials auch nach direktem Kontakt mit Flüssigstickstoff. Das Etikett delaminiert nicht, wenn Kondensat entsteht – und der DataMatrix-Code bleibt nach dem Auftauen scanfähig.

Dokumentenfolie
Rohstoffbehälter, Laborgeräte und Kalibrierungsnachweise brauchen Kennzeichnungen, die über Jahre lesbar bleiben. Dokumentenfolie besteht aus Polyesterfolie mit hoher Chemikalienresistenz. Sie haftet dauerhaft, löst sich bei Manipulationsversuchen erkennbar ab und erfüllt GMP-Dokumentationspflichten für Chargennachverfolgung und Langzeitarchivierung.

Mehrlagen-Etiketten
Kleine Ampullen und Vials tragen FMD-Pflichtangaben, Dosierdaten und Warnhinweise – oft in mehreren Sprachen. Auf der verfügbaren Fläche ist das ohne aufklappbare Innenlagen nicht lösbar. Mehrlagen-Etiketten bieten erweiterte Informationskapazität auf kleinstem Format, ohne dass der DataMatrix-Code oder die Pflichtfelder auf dem Obermaterial weichen müssen.

Autoklavierbare Etiketten
Glasvials und sterilisierbare Medizinprodukte durchlaufen Dampfsterilisation bei 121 °C oder 134 °C. Standard-Etiketten verlieren dabei Haftkraft oder zeigen Dimensionsveränderungen. Autoklavierbare Etiketten bestehen diese Zyklen ohne Druckverlust und ohne Kleberaustritte – der GMP-konforme Klebstoff migriert nicht in den Primärpackungsbereich.

Booklet-Etiketten
Wo der vollständige Beipackzettel auf der Primärverpackung integriert sein muss, bietet das Booklet-Etikett die notwendige Seitenanzahl direkt auf der Packung. Das gebundene Format haftet sicher auf der Verpackungsoberfläche, die Textseiten lassen sich aufklappen und wieder verschließen. Geeignet für Arzneimittel mit umfangreichen mehrsprachigen Pflichtangaben.
Fünf technische Anforderungen vor der Materialentscheidung klären
Pharmazeutische Etiketten scheitern selten an offensichtlichen Fehlern. Sie scheitern, weil ein Parameter unter realen Prozessbedingungen nicht bekannt war – der Druck beim Autoklavieren, die Oberflächenenergie des Kunststoffs oder der Kontrast des DataMatrix-Codes auf dem spezifischen Folienmaterial. Diese fünf Punkte helfen, die Anforderungen Ihrer Anwendung vor der Materialauswahl vollständig zu erfassen.
Substrat und Oberflächeneigenschaften
• Auf welchem Material haftet das Etikett – Glas, PE, PET, Aluminium oder Papier?
• Gibt es eine Oberflächenbeschichtung oder Behandlung, die die Haftung beeinflusst?
• Wird das Substrat vor der Etikettierung gereinigt oder desinfiziert?
Temperatur- und Sterilisationsbedingungen
• Durchläuft die Verpackung Dampfsterilisation, Ethylenoxid-Behandlung oder Tiefkühllogistik?
• Bei welcher Temperatur und welchem Druck findet die Sterilisation statt?
• Entsteht Kondensat beim Auftauen oder beim Wechsel zwischen Temperaturzonen?
Chemische Einwirkungen im Prozess
• Welche Desinfektionsmittel oder Reinigungschemikalien kommen mit dem Etikett in Kontakt?
• Gibt es Lösungsmittelkontakt in der Produktions- oder Laborumgebung?
• Welche pH-Werte treten bei CIP-Prozessen oder Reinigungszyklen auf?
DataMatrix-Druck und EMVS-Verifikation
• Welches Druckverfahren und welche Auflösung setzt Ihre Produktionslinie ein?
• Wurde der Mindestkontrast von 40 % auf dem tatsächlichen Folienmaterial geprüft?
• Ist eine 100 %-Inline-Prüfung jedes DataMatrix-Codes in der Linie vorgesehen?
Informationskapazität und Verpackungsfläche
• Müssen FMD-Pflichtangaben, Warnhinweise und Dosierdaten auf der Primärverpackung untergebracht werden?
• Sind mehrsprachige Angaben erforderlich, die die verfügbare Fläche überschreiten?
• Gibt es eine Anforderung für integrierte Beipackzettel oder aufklappbare Innenlagen?
Häufig gestellte Fragen – Pharmazeutische Industrie
Nach dem dritten Autoklavierdurchgang zeigen sich die Unterschiede. Standard-Klebstoffe verlieren bei 121 °C Haftung oder migrieren an die Substratoberfläche – beides ist GMP-kritisch. Unsere Folienmaterialien für Sterilisationsanwendungen behalten ihre Dimensionsstabilität und überstehen mehrere Zyklen ohne Kantenablösung. Der Klebstoff bleibt innerhalb der definierten Schicht. Kleberaustritte in den Primärpackungsbereich treten dabei nicht auf. Wie viele Zyklen Ihr spezifischer Prozess verlangt und bei welchem Druck – das bestimmt, welches Material passt. Testen Sie das auf Ihren eigenen Vials unter Ihren Prozessbedingungen. Unser Technologie-Team bespricht mit Ihnen vorab, welche Materialkombination für Ihre Zyklenanzahl und Temperatur geeignet ist.
PE gehört zu den Kunststoffen mit niedriger Oberflächenenergie. Normaler Klebstoff zieht sich beim ersten Temperatursturz zurück. Das Kondensat beim Auftauen verstärkt das – das Etikett hebt an den Kanten ab, der DataMatrix-Code wird unlesbar. Materialien für Kryoanwendungen nutzen Haftsysteme, die gezielt auf niedrigenergetische Oberflächen ausgelegt sind. Sie haften direkt nach der Applikation, ohne Vorbehandlung des Röhrchens. Nach dem Kontakt mit Flüssigstickstoff und erneutem Auftauen zeigt das Obermaterial keine Einbußen bei Lesbarkeit oder Randklebekraft. Ob das auf Ihrem spezifischen Röhrchentyp ebenso gilt, prüfen Sie an Ihren eigenen Gebinden – das Technologie-Team begleitet Sie dabei mit gezielter Materialauswahl.
FMD verlangt einen DataMatrix-Code, der am Point of Sale gescannt wird – nicht nur in der Produktion. AMG §10 schreibt Pflichtangaben vor, die dauerhaft lesbar sein müssen. Unsere Lösungen unterstützen beide Anforderungen durch aufeinander abgestimmte Druck- und Folienmaterialkombinationen. Der DataMatrix-Code hält auf dem Obermaterial auch nach Kühlkettenpassage seinen Kontrast. Die Chargendokumentation, die wir mitliefern, ist für Compliance-Nachweise im Audit verwertbar. Wo mehrsprachige Pflichtangaben auf kleinen Primärverpackungen nicht flächig unterzubringen sind, bieten Mehrlagen-Varianten die notwendige Informationskapazität. Welche Variante Ihre spezifische Verpackung braucht, klären Sie am besten direkt mit unserem Technologie-Team.
Die meisten Etikettierlinien in der Pharmaproduktion arbeiten mit Thermal-Transfer-Druck oder vorgedruckten Rollen. Beide Varianten funktionieren mit unseren Folienmaterialien – entscheidend ist die Rollengeometrie, der Kerndurchmesser und die Materialstärke. Wenn Ihre Linie mit engem Etikettieraggregat arbeitet, spielt auch die Steifigkeit des Materials eine Rolle. Zu dünne Lagen rutschen, zu dicke blockieren den Spender. Wir kennen die gängigen Anlagenkonfigurationen und stimmen die Materialgeometrie darauf ab. Ihr Maschinenbauer muss dabei nicht involviert werden. Für die Inline-Prüfung des DataMatrix-Codes gilt: Die Druckqualität auf dem jeweiligen Folienmaterial bestimmt, ob Ihr Kamerasystem sauber ausliest – das zeigt sich im Betrieb auf Ihrer Linie.
Kein Datenblatt ersetzt den Test auf dem echten Substrat unter echten Prozessbedingungen. Ein Material, das auf Borosilikatglas bei 121 °C besteht, muss auf Ihrem Vial-Typ mit Ihrer Befüllung nicht identisch abschneiden. Füllgut, Restfeuchte im Autoklav und Kammergeometrie beeinflussen das Ergebnis. Der richtige Weg: Sie applizieren das Mustermaterial auf Ihren eigenen Gebinden und führen die Belastungszyklen durch, die Ihre Produktion vorgibt. Wir liefern das Material und unterstützen Sie mit konkreten Empfehlungen, worauf Sie beim Test achten sollten – Kantenablösung, Drucklesbarkeit, Kleberrückstand. Was Sie dabei dokumentieren, fließt direkt in Ihren Qualifizierungsnachweis ein. So entsteht eine Entscheidungsbasis, die Ihrer Validierung standhält.
